政府支持
审评审批支持:国家对医疗器械审评审批制度进行改革,审评审批资源更多向临床急需的重点创新药和医疗器械倾斜。对于康氧公司涉及的相关产品,在临床试验、注册申报等全过程可能会得到更高效的沟通交流和个性化指导,加快产品上市进程。
标准引领:深入推进国家药品医疗器械标准提高行动计划,积极推进新技术、新方法、新工具的标准研究和转化。这有助于公司参与相关标准的制定和完善,提升公司在行业内的影响力,同时也为公司产品的研发和生产提供更明确的标准和规范。
知识产权保护:完善药品医疗器械知识产权保护相关制度,对符合条件的产品给予一定的数据保护期和市场独占期。康氧公司的细胞系产品如果涉及相关创新成果,将能够得到知识产权方面的保护,鼓励公司进行技术创新和产品研发。
医保支持:坚持基本医疗保险 “保基本” 功能定位,完善医保药品目录调整机制,按程序将符合条件的创新药和医疗器械纳入医保支付范围。如果康氧公司的产品能够与相关医保政策相结合,将有助于扩大产品的市场应用范围,提高产品的可及性。
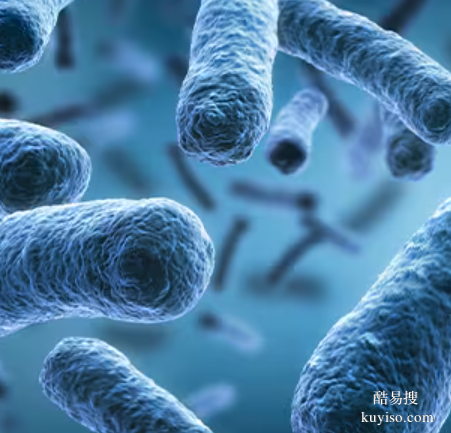
标准化培养:严格按照美国药典(USP)等相关规范中推荐的方法和条件进行菌株的培养。包括选择合适的培养基、培养温度、培养时间等,以确保菌株能够在最适宜的环境中生长,维持其生物学特性的稳定性。
多样化保存:采用多种保存方法,如低温冷冻干燥、液氮贮存、超低温冷冻(低于 -30℃)等,以满足不同菌株的保存需求。对于一些对保存条件要求较高的菌株,会进行特殊的处理和保存,例如某些厌氧菌需要在无氧条件下进行冷冻保存。同时,会对保存的菌株定期进行复苏和检查,确保其在保存过程中没有发生变异或死亡。
批次间一致性的保证
质量管理体系认证:无论是保藏机构还是检测机构,通常需要建立并运行有效的质量管理体系,并通过相关认证。如 ISO 9001 质量管理体系认证,表明机构在管理职责、资源管理、产品实现和测量、分析与改进等方面具备完善的管理机制,能够保证标准菌株来源确认工作的规范性和一致性。对于微生物检测实验室,还可能需要通过 ISO 15189《医学实验室 - 质量和能力的专用要求》认证,针对医学实验室的特殊要求进行规范,确保在临床诊断等领域标准菌株来源确认的质量和可靠性。
溯源体系认证:为了确保标准菌株来源的可追溯性,一些机构可能会建立溯源体系,并寻求相关认证。例如,依据 GS1 全球追溯标准等建立的溯源系统,通过对标准菌株从采集、保藏、检测到使用等各个环节进行信息记录和标识,实现对菌株来源的准确追溯。通过相关溯源体系认证,可证明机构在菌株来源确认和追溯方面具备完善的能力和管理水平。
不同国家和地区对于标准菌株来源确认的资质和认证要求可能会有所差异,具体要求需根据当地的法律法规、行业标准以及相关机构的规定来确定。

1、为了您的资金安全,请选择见面交易,任何要求预付定金、汇款等方式均存在风险,谨防上当受骗!
2、确认收货前请仔细核验产品质量,避免出现以次充好的情况。
3、该信息由酷易搜网用户自行发布,其真实性及合法性由发布人负责,酷易搜网仅引用以供用户参考,详情请阅读酷易搜网免责条款。
查看详情>
关键词:杭州0代标准菌株,菌株,杭州菌株,菌株价格